Связаться с приемной комиссией
Меню раздела
Основное меню
Множественная миелома является одним из видов рака крови, при котором поражаются плазматические клетки внутри костного мозга. При множественной миеломе костным мозгом вырабатывается огромное количество аномальных плазматических клеток, которые препятствуют нормальному функционированию костного мозга и разрушают окружающие костные структуры. Чаще всего при множественной миеломе поражаются позвоночник, череп, таз и ребра. Специфическое лечение наиболее часто включает комбинацию обычной химиотерапии и одного или более дополнительных препаратов, таких как ингибиторы протеасом и иммуномодулирующие препараты.
Бортезомиб является одним из наиболее распространенных и широко используемых на протяжении последних 20 лет ингибиторов протеасом. Протеасомы - ферменты, которые находятся во всех клетках и играют важную роль в функции и росте клеток. Протеасома 26S находится в ядре клеток и является ключевым компонентом, катализирующим расщепление основных белков, участвующих в управлении жизненным циклом клеток. Ингибирование протеасомы приводит к апоптозу (гибели) клетки. При этом миеломные клетки почти в 1000 раз более восприимчивы к апоптозу, вызванному бортезомибом, чем нормальные клетки плазмы. Тем не менее, бортезомиб имеет ряд недостатков, ограничивающих его применение. Во-первых, бортезомиб является достаточно токсичным веществом, что лимитирует возможные дозы препарата. Однако даже ограниченные дозы препарата приводят к ряду нежелательных побочных эффектов, вызываемых воздействием на здоровые ткани. Во-вторых, бортезомиб имеет низкую биодоступность, основной причиной которой является низкая растворимость его в водных средах.
Для решения данных проблем коллективом ученых РХТУ им. Д.И. Менделеева совместно с коллегами из МГУ им. Ломоносова, ИБХ РАН, НМИЦ "Онкологии им. Н.Н. Блохина", РУДН, Сеченовского Университета, Университета Фессалии и Критского Университета (Греция) был разработан наноразмерный носитель лекарства на основе модифицированного амфифильного (имеющего гидрофобную и гидрофильную части молекулы) поливинилпирролидона (ПВП). Полученное производное ПВП имеет хорошую способность к солюбилизации гидрофобных лекарственных веществ, повышая их водосовместимость и биодоступность, низкотоксичен и экологичен. Полученная полимерная система представляет из себя сферические наночастицы с диаметром в диапазоне от 290 до 330 нанометров, в которых молекулы бортезомиба формируют условное «ядро» в результате взаимодействия с гидрофобными частями молекул амфифильного ПВП.
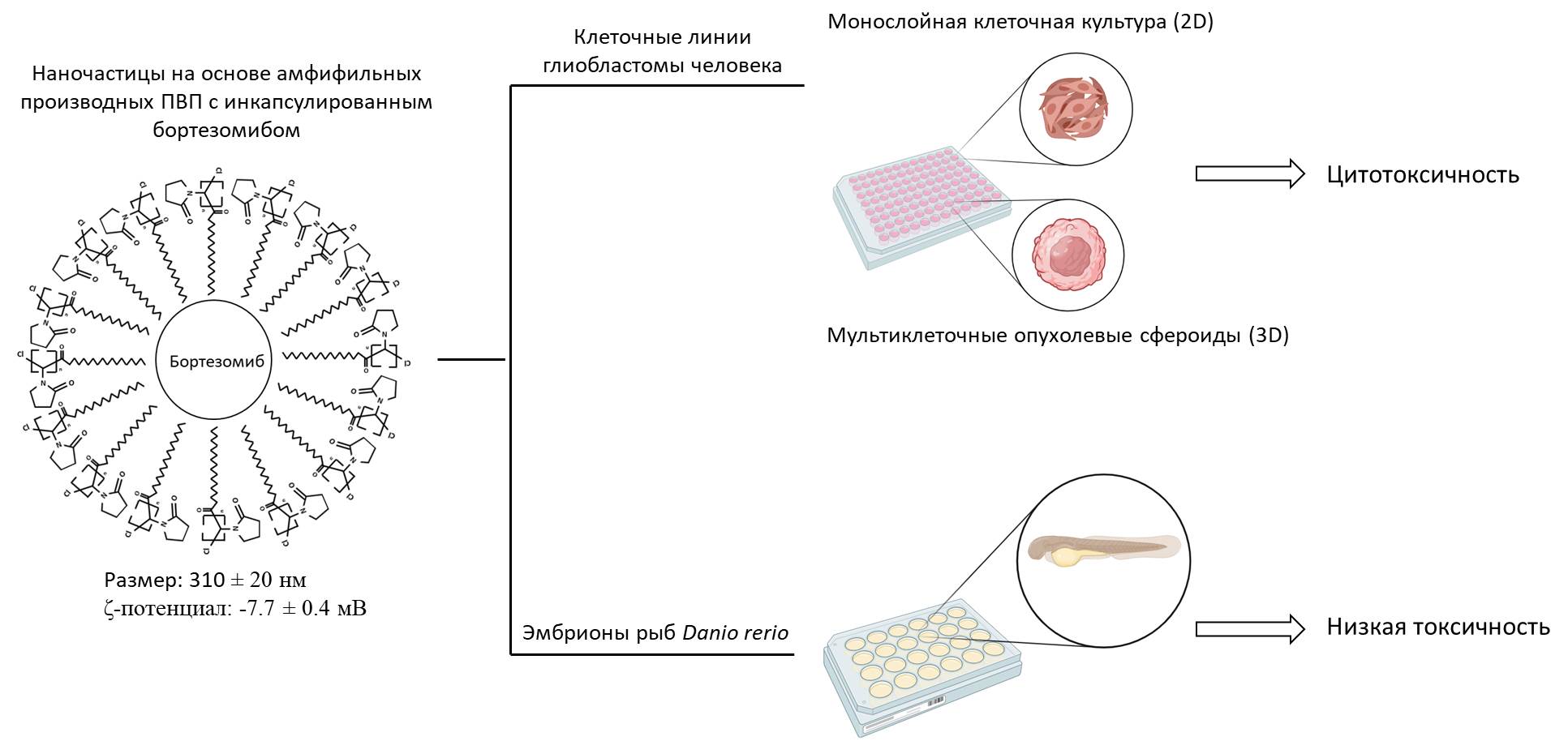
Благодаря полимерному носителю у лекарственного препарата не только снижаются побочные эффекты, но и улучшается общая эффективность благодаря более селективному и продолжительному воздействию. Кроме того, по словам авторов, такой препарат может применяться не только для лечения множественной миеломы, но и против других злокачественных образований. В качестве подтверждения данной гипотезы было проведено исследование эффективности препарата против клеток глиобластомы, продемонстрировавшее эффективность против клеток опухоли и относительную безопасность для здоровых клеток. В дополнение к этому было проведено изучение токсичности препарата на эмбрионах рыб Данио-рерио. Полученные значения концентрации полулетальной дозы препарата на порядок превосходят концентрацию полумаксимального ингибирования раковых клеток, что говорит о существовании терапевтического «окна» концентраций между эффективной дозой и токсичностью, ограничивающей дозировку лекарственного средства.
.png)
Тем не менее, авторы отмечают, что методология исследования, проведенного на эмбрионах Данио-рерио, имеет определенные ограничения ввиду значительного отличия биологии рыб от млекопитающих. Дальнейшие исследования позволят получить более подробную информацию о фармакокинетических параметрах препарата, эффективности против опухолей и безопасности для здоровья животных и человека. Также в качестве перспективного направления будущих исследований авторы отмечают возможность модификации поверхности полимерной оболочки наночастиц специально синтезируемыми ими противоопухолевыми векторными молекулами белковой природы для улучшения эффективности адресной доставки лекарственного препарата и усиления его комбинированного действия на раковые клетки.
.png)
Исследования были проведены в рамках гранта Российского научного фонда № 23-15-00468.